А.С. Аметов, А.В. Жигарева,
Е.Ю. Пашкова, З.Д. Рамазанова
Российская медицинская академия непрерывного профессионального образования
Городская клиническая больница им. С.П. Боткина, Москва
Введение
Заболеваемость сахарным диабетом (СД) 2 типа во всем мире неуклонно возрастает. Следовательно, будет увеличиваться количество лиц, страдающих сердечно-сосудистыми заболеваниями. В настоящее время установлено, что СД 2 типа ассоциируется с наличием клинически выраженной сердечно-сосудистой патологии. У пациентов с СД 2 типа повышен риск развития ишемической болезни сердца, инфаркта миокарда, острого нарушения мозгового кровообращения, артериальной гипертензии. Кроме того, сердечно-сосудистые заболевания признаны ведущей причиной смерти таких пациентов. Так, показатели смертности у страдающих СД в шесть – десять раз выше, чем у лиц без указанной патологии [1]. Именно поэтому внимание ученых и врачей направлено на поиск возможностей существенно уменьшить смертность и увеличить продолжительность жизни больных СД 2 типа. Одним из таких инструментов могут стать ингибиторы натрий-глюкозного котранспортера 2 (иНГЛТ-2).
В сентябре 2015 г. в Стокгольме были представлены результаты крупного рандомизированного клинического исследования EMPA-REG OUTCOME. Согласно полученным данным, на фоне терапии эмпаглифлозином риск основных неблагоприятных сердечно-сосудистых событий (смерти от сердечно-сосудистых заболеваний, нефатального инфаркта и инсульта) снизился на 14% [2].
Для оценки сердечно-сосудистых эффектов иНГЛТ-2 не менее важны результаты исследований CANVAS и CANVAS – Renal. В них изучалось влияние канаглифлозина на риск развития сердечно-сосудистых и почечных осложнений. Препарат снижал риск наступления конечной комбинированной точки (смерти от сердечно-сосудистых заболеваний, нефатального инфаркта и инсульта) на 14% [3].
Положительное действие дапаглифлозина на сердечно-сосудистые исходы доказано в исследовании фазы III DECLARE-TIMI 58. В частности, данный препарат снижал риск достижения первичной комбинированной точки – госпитализации по причине сердечной недостаточности и сердечно-сосудистой смерти на 17% [4].
Необходимо отметить, что механизмы, которые привели к подобным результатам, до конца не изучены. В настоящее время существует ряд концепций, объясняющих данный феномен.
В перечисленных выше исследованиях иНГЛТ-2 оказались эффективными не только в отношении показателей углеводного обмена и сердечно-сосудистой безопасности, но и продемонстрировали положительные негликемические эффекты – в частности, снижение массы тела, измеренной в килограммах. Увеличивая экскрецию глюкозы с мочой, они способствовали выведению из организма лишних калорий и, следовательно, снижению массы тела в среднем на 2 кг [5]. В условиях относительного дефицита глюкозы иНГЛТ-2 запускают процесс утилизации липидов и кетогенез в качестве преобладающего субстрата. Это метаболическое изменение является основным механизмом потери веса, опосредованной иНГЛТ-2. В то же время о влиянии иНГЛТ-2 на уровни адипонектина и лептина в плазме крови доказательств пока не получено. Тем не менее подобно Робин Гуду иНГЛТ-2 активируют неиспользованное богатство липидов и экономят «изнуренный метаболизм» глюкозы, уменьшая инсулинорезистентность и изменяя энергетический механизм в организме [6].
Анализируя возможные механизмы достижения впечатляющих сердечно-сосудистых исходов на фоне приема иНГЛТ-2, мы посчитали необходимым наряду с параметрами гликемического контроля и антропометрическими данными, такими как вес, окружность талии (ОТ), индекс массы тела (ИМТ), одномоментно изучить показатели, характеризующие жировой метаболизм. Основными среди них считаются лептин и адипонектин. Уровень первого четко коррелирует с динамикой массы тела. Второй является ключевым маркером метаболического здоровья.
Целью нашей работы стала оценка влияния ингибитора натрий-глюкозного котранспортера 2 канаглифлозина на углеводный и жировой обмен у пациентов с СД 2 типа и висцеральным ожирением.
Клинический случай 1
Пациент Р., 67 лет, наблюдался у эндокринолога по поводу СД 2 типа. Патология выявлена в 2012 г. Больной принимал метформин 850 мг два раза в день, диету не соблюдал, самоконтроль глюкозы проводил нерегулярно. Жаловался на сухость во рту, жажду, периодические отеки нижних конечностей, онемение и парестезию нижних конечностей.
Госпитализирован в эндокринологический стационар.
Диагноз: СД 2 типа, дистальная диабетическая сенсомоторная полинейропатия, экзогенно-конституциональное ожирение первой степени. Целевой уровень гликированного гемоглобина (HbA1c) < 7,0%.
В первые дни госпитализации проведено непрерывное мониторирование глюкозы в крови (рис. 1). Выявлена значительная вариабельность гликемии, что свидетельствовало о наличии глюкозотоксичности.
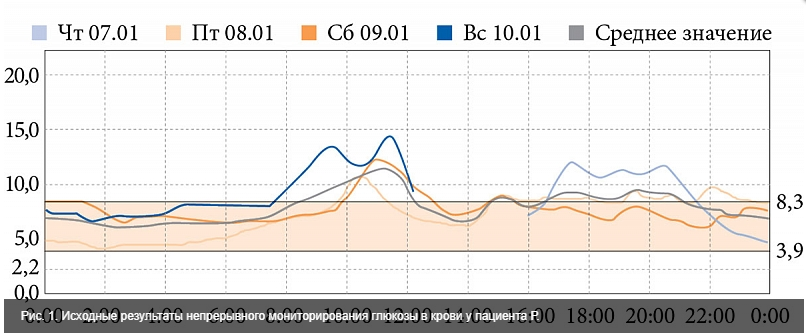
Рекомендована комбинированная сахароснижающая терапия – канаглифлозин 100 мг и метформин 2000 мг.
Через шесть месяцев терапии канаглифлозином и метформином у пациента удалось достичь целевых значений гликемических параметров, таких как глюкоза плазмы натощак (ГПН), постпрандиальная гликемия (ППГ) и HbA1c. В частности, уровень глюкозы плазмы натощак снизился с 10,1 до 5,2 ммоль/л, через два часа после еды – с 14,5 до 5,8 ммоль/л, HbA1c – с 9,5 до 6,0% (рис. 2).
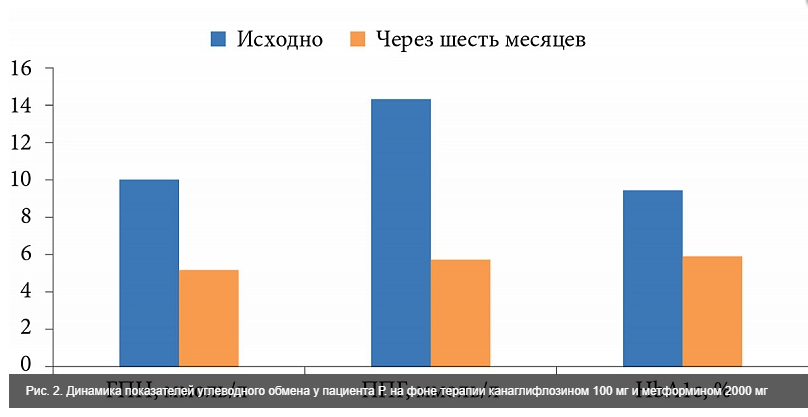
Согласно результатам повторного непрерывного мониторирования глюкозы, проведенного через шесть месяцев, значения глюкозы практически приблизились к физиологическим (рис. 3). Это позволило полностью нейтрализовать глюкозотоксичность.
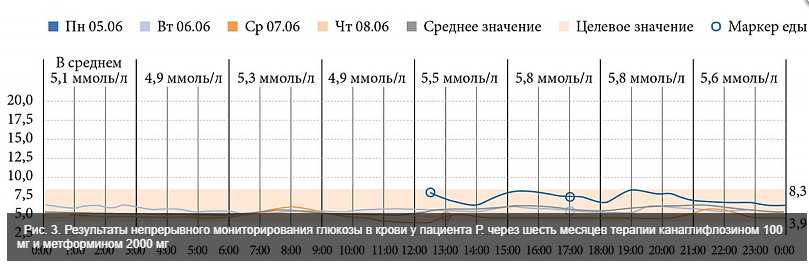
Важно отметить, что, «убрав лишнюю глюкозу», нейтрализовав глюкозотоксичность, мы получили снижение всех антропометрических показателей. Так, за время наблюдения масса тела уменьшилась на 10 кг, ИМТ – на 3 кг/м2, ОТ – на 14 см.
Для изучения влияния терапии иНГЛТ-2 на показатели метаболического здоровья у пациента был определен уровень лептина, а также адипонектина в плазме крови.
На фоне снижения антропометрических показателей отмечено пропорциональное уменьшение уровня лептина (с 15,2 до 5,1 нг/мл) и обратно пропорциональное повышение уровня адипонектина (с 11,4 до 15,0 мкг/мл) (рис. 4).
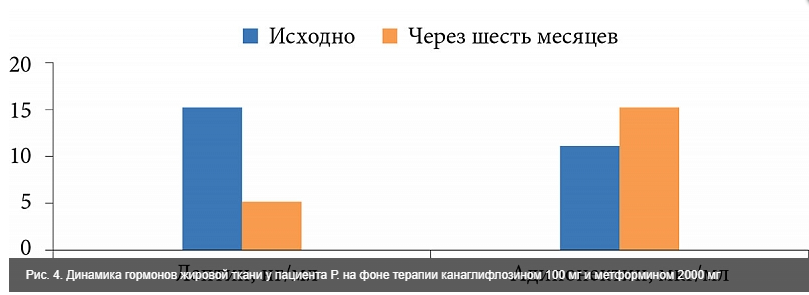
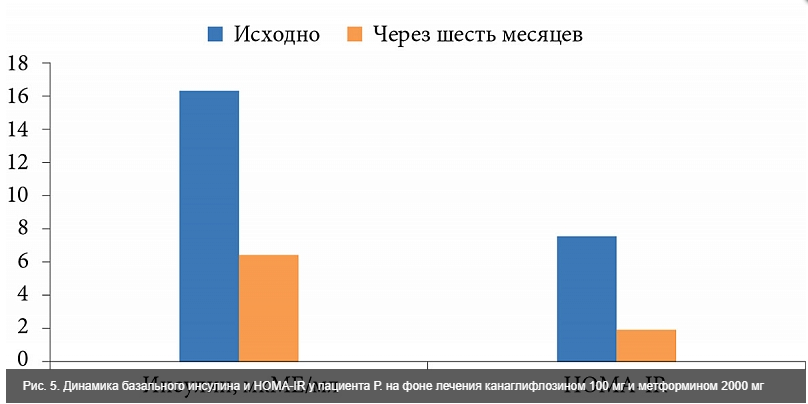
Известно, что адипонектин обладает рядом метаболических эффектов, в частности его уровень коррелирует с чувствительностью тканей к инсулину. Так, у пациента Р. в результате увеличения уровня адипонектина секреция базального инсулина уменьшилась с 16,5 до 6,3 мкМЕ/мл, значения индекса гомеостатической модели оценки резистентности к инсулину (Homeostasis Model Assessment of Insulin Resistance – HOMA-IR) – с 7,47 до 1,96 (рис. 5).
Следует отметить, что в разных клинических исследованиях были получены данные о том, что канаглифлозин в дозе 300 мг/сут помимо ингибирования НГЛТ-2 в проксимальных почечных канальцах способен уменьшать абсорбцию глюкозы в кишечнике посредством локального и переходящего ингибирования НГЛТ-1. Этим механизмом обусловлено его положительное влияние на постпрандиальную гликемию [6].
Клинический случай 2
Данный клинический случай демонстрирует возможности разнонаправленного действия канаглифлозина в дозе 300 мг/сут.
Пациент П., 51 год, был доставлен в эндокринологический стационар больницы скорой медицинской помощи. Больной жаловался на сухость во рту, жажду, учащенное мочеиспускание (до двух-трех раз за ночь), снижение зрения. Гликемия повысилась до 14 ммоль/л.
Состояние ухудшилось в течение последнего месяца. Повышение гликемии зафиксировано впервые, у эндокринолога ранее не наблюдался.
На момент осмотра рост больного составлял 177 см, масса тела – 120 кг, ИМТ – 38,7 кг/м2, ОТ – 123 см, артериальное давление – 140/90 мм рт. ст., частота сердечных сокращений – 86 в минуту.
Показатели углеводного обмена: HbA1c – 7,9 (норма – 6,5)% – нецелевой уровень для пациента, гликемия натощак – 12,6 (4,4–6,5) ммоль/л, постпрандиальная гликемия – 11,2 (4,4–8,0) ммоль/л, метаболического здоровья: лептин – 19,2 (3,7–11,1) нг/мл, адипонектин – 36,6 (10,0–20,0) мкг/мл. Инсулин – 4,0 мкЕд/мл, индекс НОМА-IR – 2,5.
Диагноз: впервые выявленный СД 2 типа, экзогенно-конституциональное ожирение второй степени, артериальная гипертензия второй стадии второй степени четвертой группы риска. Целевой уровень HbA1c < 6,5%.
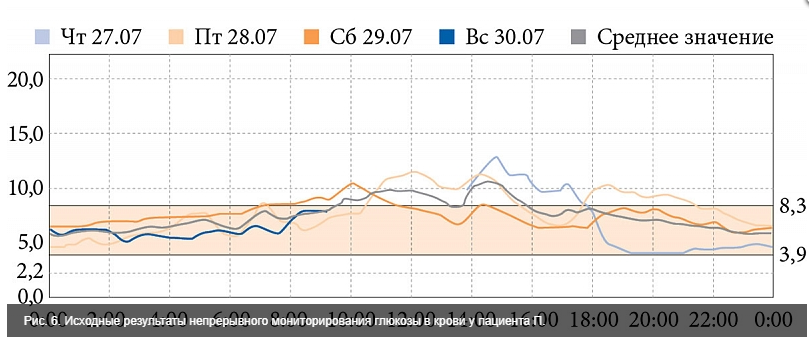
В первые дни госпитализации проведено непрерывное мониторирование глюкозы. Полученные результаты свидетельствовали о наличии гипергликемии преимущественно с 09:00 до19:00 (рис. 6).
Для уменьшения глюкозотоксичности проведен курс инсулинотерапии в базисно-болюсном режиме, после чего принято решение о переводе больного на пероральные сахароснижающие препараты. Принимая во внимание удовлетворительные показатели функции почек (скорость клубочковой фильтрации – 68 мл/мин/1,73 м2), ожирение с преимущественным отложением подкожно-жировой клетчатки в области живота, тенденцию к повышению постпрандиальной гликемии, были назначены канаглифлозин 300 мг (утром) и метформин 1000 мг два раза в день. Последний является препаратом первой линии у пациентов с впервые выявленным СД 2 типа.
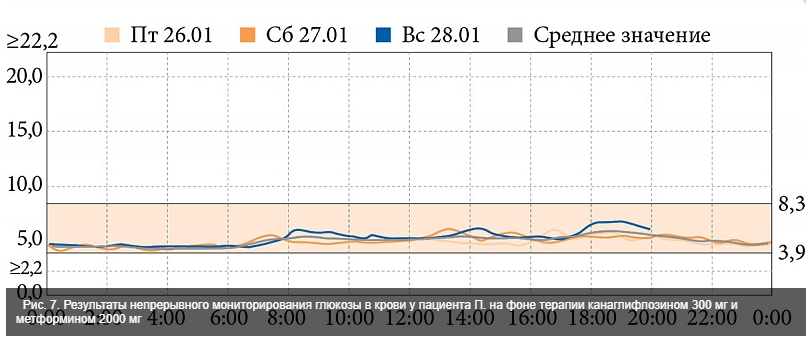
Через шесть месяцев на фоне проводившегося лечения отмечена положительная динамика по ряду клинико-лабораторных показателей. Снизились антропометрические параметры: масса тела – на 12,3 кг, ИМТ – на 3,4 кг/м2, ОТ – на 12 см. Показатели углеводного обмена также уменьшились: HbA1c – на 3,0%, гликемия натощак – на 7,7 ммоль/л, постпрандиальная гликемия – на 4,6 ммоль/л. Согласно результатам непрерывного мониторирования глюкозы в течение трех дней, значительно уменьшилась вариабельность гликемии за счет снижения постпрандиального уровня глюкозы. В 09:00 и 14:00 у пациента был полноценный прием пищи, канаглифлозин нивелировал риск возникновения гипергликемии и глюкозотоксичности (рис. 7).
На фоне нормализации гликемических и антропометрических показателей у больного снизился уровень лептина – на 15,0 нг/мл, уровень адипонектина, наоборот, повысился – с 36,6 до 61,8 мкг/мл. Кроме того, наблюдалось уменьшение индекса НОМА-IR – на 1,5.
Заключение
Использование канаглифлозина как для интенсификации, так и на старте терапии СД 2 типа способствует нормализации углеводного обмена и нейтрализации глюкозотоксичности. Кроме того, такое лечение приводит к снижению массы тела, индекса массы тела и окружности талии, восстановлению баланса ключевых показателей жирового обмена – лептина и адипонектина. Вследствие повышения уровня адипонектина улучшается чувствительность тканей к инсулину.
Источник: Журнал “Эффективная фармакотерапия”. 2019.Том 15. № 22. Эндокринология
