Сахарный диабет
Заболевание, о котором слышал даже последний троечник. Суть его в том, что имеющаяся в крови глюкоза не может проникнуть в клетки инсулинзависимых тканей (таких как жировая и мышечная). Вся беда из-за инсулина: либо его нет, либо по каким-то причинам он не действует на клетку (не секретируется должным образом; «сломались» инсулиновые рецепторы в клетке или мутировали гены протеинкиназ, ответственных за пострецепторную передачу с инсулиновых рецепторов, — да мало ли причин). Бывает так, что усиливается действие контринсулярных гормонов: глюкагона, глюкокортикостероидов (так, выделяют даже глюкокортикостероидный сахарный диабет). Бывает, что диабет становится «продолжением» иной патологии — в наихудшем случае диабет оказывается проявлением очень опасного и трудно поддающегося лечению заболевания — рака поджелудочной железы.
Классификация сахарного диабета на сегодняшний день является чрезвычайно широкой, хотя она и не претерпела существенных изменений с 1999 года (расширились лишь представления о других специфических формах сахарного диабета).

Сахарный диабет имеет множество причин, и представления об этом заболевании выходят далеко за рамки деления на диабет I и II типов. И чтобы понять, что вообще происходит при сахарном диабете, разберемся с ролью инсулина в метаболических процессах.
Механизм действия инсулина
Все, что делает инсулин с метаболизмом, направлено на выживание клетки, на ассимиляционные и пластические процессы (анаболизм). По разным данным, эффект инсулина основан на его действии на соответствующие мембранные рецепторы, обладающие тирозинкиназной активностью. Дальнейшие изменения связаны с активностью рецептора и фосфорилированием его субстратов. И здесь начинается самое интересное и самое сложное.
Внутриклеточные изменения при активации инсулинового рецептора развиваются по двум направлениям — фосфатидилинозитол-3-киназному и по МАРК-пути (см. главу 2).
События, связанные с образованием фосфатидилинозитол-3,4,5-триcфосфата, запускают в клетке метаболические изменения, которые затрагивают все виды обмена веществ. Посредником этих изменений выступает ось протеинкиназа В (АКТ) — mTOR (мишень рапамицина). Данная ось работает в нескольких направлениях:
- изменения в транскрипции ДНК и экспрессии белков, включенных в метаболические процессы;
- перемещение переносчика глюкозы GLUT 4 в клеточную мембрану;
- изменения концентрации цАМФ в клетке и модуляция активности различных ферментов в клетке.
Все это порождает метаболические ответы в клетке. Проследим же их [1, 3, 5].
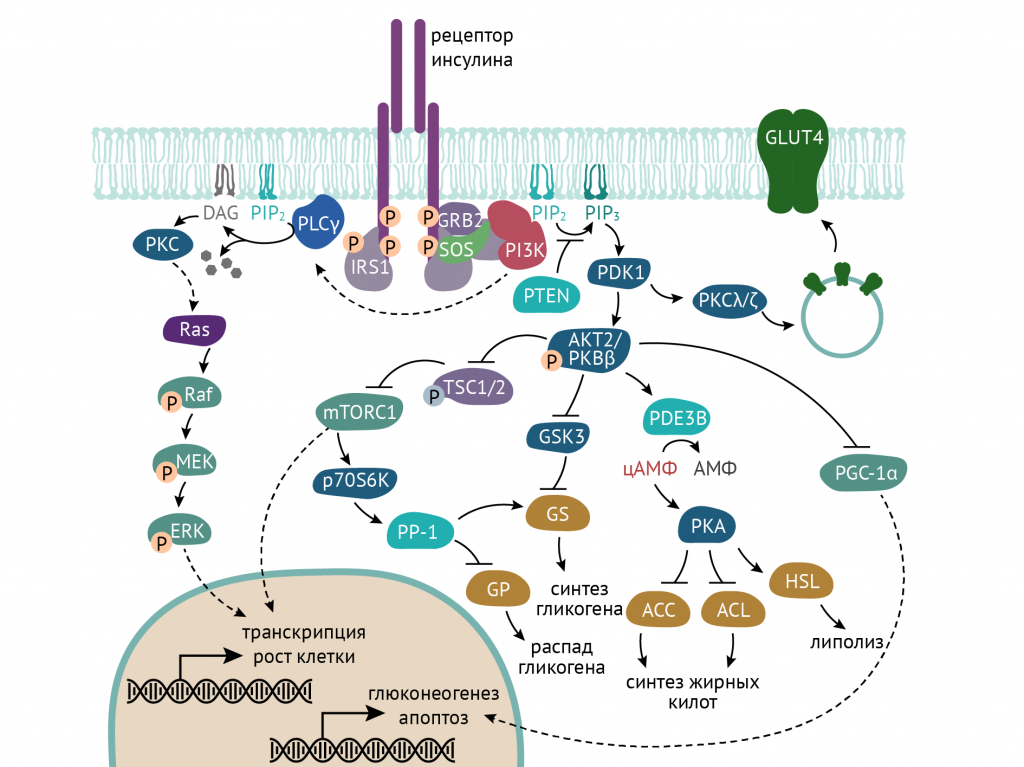
Изменения углеводного метаболизма
В целом, сводятся к повышению утилизации клетками глюкозы:
- AKT2-зависимая транслокация переносчиков глюкозы GLUT4 в плазматическую мембрану клетки. Это событие обеспечивает поступление глюкозы в инсулинзависимые ткани — мышечную и жировую.
- Торможение распада гликогена путем ингибирования фосфорилазы гликогена вследствие активации гликогенсинтазы (см. схему выше).
- AKT-зависимая активация ключевого фермента гликолиза — фосфофруктокиназы, а по ряду данных — еще и гексокиназы.
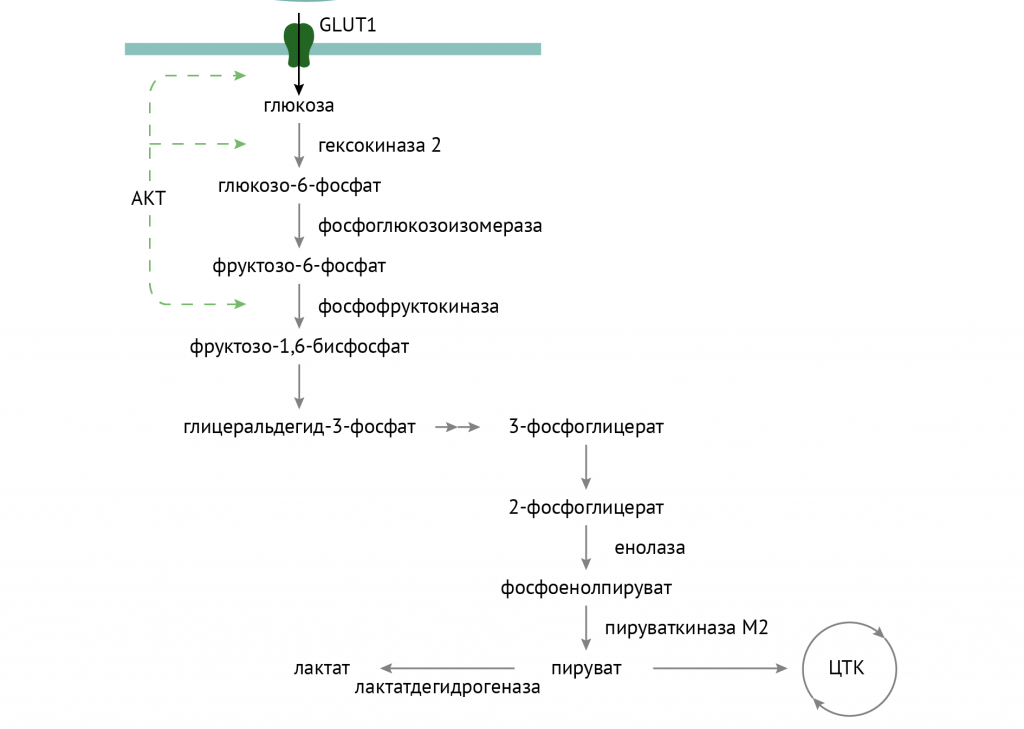
- Торможение процессов глюконеогенеза. Реализуется это как аллостерическим ингибированием фруктозо-1,6-бифосфатазы (через цАМФ-АМФ-зависимые механизмы), так и в результате изменения транскрипции генов, кодирующих ферменты глюконеогенеза. Во многом, кстати, за счет активации аденозинмонофосфат – зависимой протеинкиназы (АМФК), которая является сенсором энергодефицита – ее активность повышается как в результате воздействия на клетку инсулина, так и в результате роста АМФ в клетке (роста соотношения АМФ к АДФ, свидетельствующее об активном использовании АТФ клеткой).
Изменения липидного метаболизма сводятся к повышению запасания ТАГ [1, 3]:
- Снижение уровня цАМФ в клетке, наблюдаемое при воздействии инсулина, уменьшает активность протеинкиназы А, необходимой для активации триацилглицеридлипазы (ТАГ-липазы). Соответственно, при действии инсулина замедляется распад ТАГ и обеспечивается их сохранение в клетке.
- Активация ключевых ферментов биосинтеза длинноцепочечных жирных кислот.
Инсулин способствует катализу на важном этапе синтеза жирных кислот, и начинается это с активации ацетил-КоА-карбоксилазы.
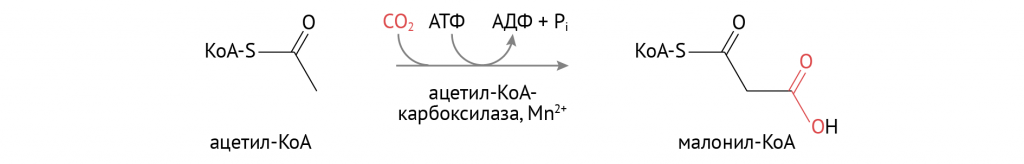
Затем малонил-КоА вовлекается в реакции биосинтеза жирных кислот, включающие в себя:
- конденсацию малых углеродных цепей;
- формирование длинной цепи, которая в конце пути станет жирной кислотой. Ниже показаны первые этапы этого во всех отношениях сложного процесса.
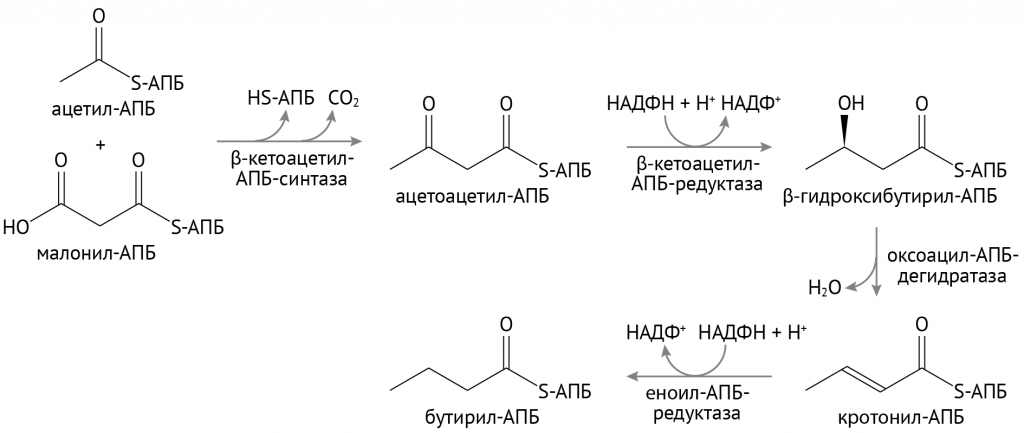
В дальнейшем образованные таким образом жирные кислоты соединяются с глицерофосфатом.
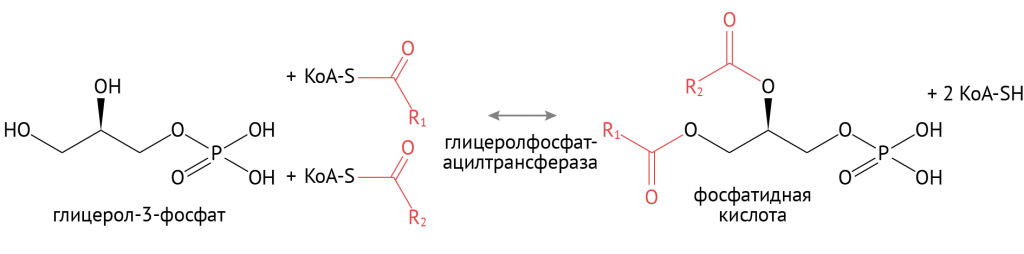
Источником глицерол-3-фосфата является уже известный тебе гликолиз. При повышенном поступлении глюкозы происходит образование множества восстановительных эквивалентов в цикле Кребса, что останавливает течение второго этапа гликолиза. Глицерол-3-фосфат в этих условиях используется для синтеза ТАГ. Именно поэтому при избыточном потреблении углеводов лишний вес — ожидаемое явление.
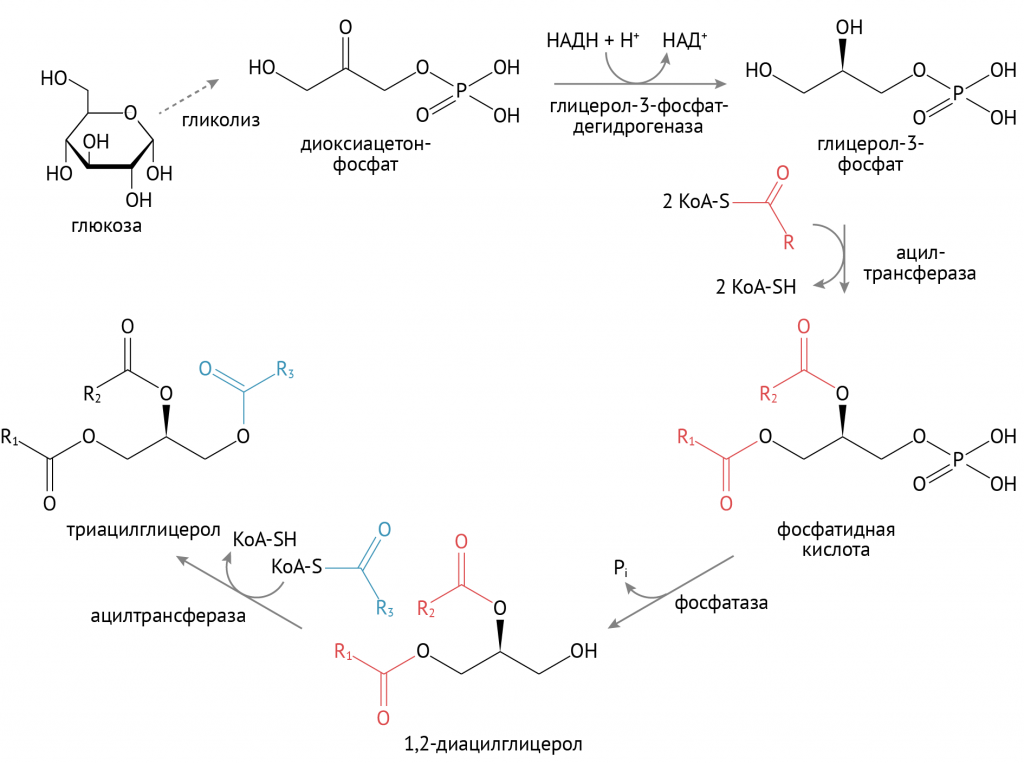
Продолжение следует…
