Влияние алкоголя на взрослый организм
Интересно, что половыми клетками дело не заканчивается. Вещества, которые мы потребляем, меняют состав крови, и растворенные в ней метаболиты могут влиять на разные органы. Например, после употребления алкоголя в крови много ацетата — он образуется в результате метаболизма спирта в печени. Ацетат проникает в мозг, где конвертируется в ацетил-KоА — субстрат для ацетилирования гистонов. Этот процесс в мозге изменяет транскрипцию (в частности, генов, отвечающих за память). Оказывается, мыши-алкоголики, которые пьют много этанола, быстрее учатся находить комнатку с этаноловой поилкой — налицо зависимость от алкоголя [36]!
Если дать алкоголь беременным мышам, ацетилирование изменится также в мозге у плода (возможно, именно это объясняет фетальный алкогольный синдром). Интересно, что источником этого ацетата может быть не только алкоголизм, но и микробы в кишечнике [37], однако как микробный метаболом влияет на его хозяев, еще только предстоит выяснить.
Как эпигенетика управляет метаболизмом: регуляция транскрипции ферментов
Интересно, что в неблагоприятных условиях среды — при недостатке самых разных метаболитов — клетки млекопитающих реагируют одинаково. Например, если в среде станет недостаточно аминокислот, активируется сигнальный путь, фосфорилирующий транскрипционный фактор (ТФ) ATF4 (не путать с АТФ!), регулирующий ферменты метаболизма аминокислот (и запускающий их синтез). Этот путь часто активируется в опухолях, которым нужно расти в условиях недостатка питательных веществ. Если ATF4 — универсальный «звонок» недостатка питательных веществ, то спусковым крючком недавно найденного транскрипционного фактора ТФ ZBTB1 служит исключительно недостаток аспарагина. Более того, недостаток этого белка приводит и к недостатку аспарагина. Эксперименты показали, что ZBTB1 непосредственно взаимодействует с промотором аспарагинсинтетазы — фермента, конвертирующего аспартат в аспарагин.
Интересно, что лейкозные клетки, в которых отсутствовал ZBTB1, чувствительны к L-аспарагиназе — ферменту, расщепляющему аспарагин и, соответственно, истощающему запасы этой аминокислоты в среде. А если лейкозные клетки без ZBTB1 подсадить мышам и лечить их L-аспарагиназой, то такие мыши живут дольше контроля [38].
Таким образом, хроматиновые белки могут регулировать метаболизм, меняя производство соответствующих ферментов, и возможно, это когда-нибудь удастся использовать в терапии заболеваний.
Как управлять циркадными ритмами, или Опять про гистоновые модификации
Как уже упоминалось, многие метилтрансферазы в качестве донора метильной группы используют S-аденозилметионин (SAM), и чем его больше — тем интенсивнее идет метилирование (и наоборот). Однако в ход идет только метильная группа, а «огрызок» SAM — S-аденозил-L-гомоцистеин (SAH) — утилизируется специальным ферментом — S-аденозил-L-гомоцистеингидролазой, играющим заодно ключевую роль в регуляции генов циркадных ритмов с партнером — транскрипционным фактором. Таким образом метаболические ферменты коллаборируют с эпигенетикой и регулируют циркадные ритмы.
Цикл сна и бодрствования регулируют циркадные ритмы. Специальные сенсорные белки реагируют на такие внешние стимулы, как свет и температура, и запускают цепочку химических превращений, приводящую к циклическому колебанию концентраций определенных метаболитов. Интересно, что белки циркадных ритмов тесно связаны с хроматином [39–41].
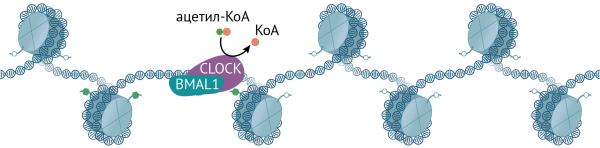
Транскрипция циркадных генов запускается ТФ CLOCK и BMAL1. Они функционируют в виде гетеродимера и связаны с изменением хроматина. Кроме того, CLOCK — это ацетилтрансфераза, ацетилирующая гистоны и другие белки (в том числе и BMAL1). Ей противостоит деацетилаза — сиртуин SIRT1, активность которого осциллирует в течение дня вослед за кофактором НАД+ [11].
S-аденозил-L-гомоцистеингидролаза взаимодействует с ТФ BMAL1, который регулирует активность циркадных генов со строгой периодичностью; в комплексе они взаимодействуют с промоторами генов. Достигается это колебанием уровня метки H3K4me3 — важной модификации активных генов на их промоторах. Интересно, что мыши, у которых эта гидролаза ингибирована в гипоталамусе, показывают уменьшенную циркадную двигательную активность, а еще у них нарушена транскрипция циркадных генов в супрахиазматическом ядре гипоталамуса (рис. 4).
Заключение
После краткого напоминания путей метаболизма мы с вами убедились, что метаболизм и эпигеном тесно связаны. Мы узнали, как замалчиваются транспозоны при недостатке метаболитов метилирования и как гомологичная рекомбинация влияет на устойчивость раковых клеток к химиотерапии. Мы узнали, что ламаркизм имеет право на существование, и что метаболиты могут влиять на половые клетки и взрослый организм, изменяя эпигенетику. Наконец, мы разобрали, как эпигеном управляет метаболизмом и как метаболизм через эпигеном регулирует цикл сна и бодрствования. В следующей, последней статье спецпроекта мы расскажем, как нарушения в эпигенетике ведут к заболеваниям.
Автор: Наталья Кочанова
