Метаболизм — совокупность химических реакций, протекающих внутри клетки, — тесно связан с эпигенетикой. Метаболиты могут влиять на молекулы, задействованные в эпигенетической регуляции, а следовательно, на все ее аспекты. В продолжении cпецпроекта об эпигенетике мы рассмотрим влияние метаболитов на организацию ядра, наследование эпигенетической информации и эпигенетические процессы. Как мы узнаем, метаболиты могут влиять как на половые, так и на соматические клетки взрослого организма (например, перепрограммировать мозг).
В предыдущих статьях спецпроекта об эпигенетике мы рассказали об организации хроматина и хроматиновых доменов [1], законах наследования эпигенетической информации [2] и процессах, протекающих на хроматине [3]. Здесь мы рассмотрим часть эпигенетического пазла, включающую метаболиты и их влияние на хроматиновую «жизнь». В нашем организме существует множество взаимосвязанных цепочек превращений одних маленьких молекул — метаболитов — в другие. Многие из них влияют на белки эпигенетической регуляции:
- Они могут быть их кофакторами: например, S-аденозилметионин (SAM) является донором метильной группы для гистонметилтрансфераз — белков, навешивающих метильные метки на гистоны [4], — а следовательно, его недостаток или избыток повлияет на метилирование.
- Они могут ингибировать эпигенетические молекулы, как, например, 2-гидроксиглутарат ингибирует некоторые гистондеметилазы — белки, снимающие метильные группы с гистонов [5].
- Они могут влиять на эпигенетические регуляторы, не будучи при этом кофакторами: например, О-ацетил-АДФ-рибоза у млекопитающих является лигандом для варианта гистона макроH2A1.1 [4], [6].
Соответственно, влияя на эпигенетические регуляторы, эти метаболиты могут запускать целые цепочки процессов на хроматине. Если всё это происходит в половых клетках, изменения передаются — как бы в противоречии идеям Дарвина — сквозь поколения! А значит, то, как мы питаемся, занимаемся ли спортом, курим и употребляем ли алкоголь — всё это может привести к эпигенетическим изменениям в наших собственных клетках, в том числе половых, и передаться детям.
Метаболиты могут влиять на клетку прямо или косвенно [4]. В первом случае они действуют на эпигенетические регуляторы непосредственно — например, кортизол (который является гормоном, но мы на него смотрим в контексте метаболизма) связывается с глюкокортикоидными рецепторами и запускает транскрипцию определенных генов; или изменение уровня SAM влияет на активность метилтрансфераз. Но может быть и непрямое влияние: метаболиты связываются с рецепторами на поверхности клеток, и тогда уже транскрипционные факторы активируются через сигнальные каскады. В этой статье мы будем говорить в основном про «прямые» метаболиты.
Многие ингибиторы эпигенетических факторов используются в исследованиях и терапии заболеваний, в том числе и разных видов рака, являясь, по сути, лекарствами [7].
В качестве введения мы кратко рассмотрим основные цепочки метаболизма, происходящие в эукариотах, и более подробно сконцентрируемся на соединениях, важных в эпигенетике.
Шпаргалка по биохимии — как меняются вещества в нашем организме
Мы рассмотрим основные цепочки превращения одних метаболитов в другие, подробно останавливаясь на процессах и соединениях, которые мы встретим дальше в статье. Для начала нужно узнать, что такое гликолиз и цикл Кребса (ведь их ингибированием удалось уменьшить эпигенетические нарушения в опухолях мозга у мышей): в ходе этих метаболических процессов получаются соединения, ведущие к другим злокачественным новообразованиям с эпигенетической основой.
Дыхание
Дыхание — это окисление определенных органических соединений до воды и углекислого газа — СО2. Если оно происходит с помощью кислорода (а ведь бывает и не так [8]), то носит название аэробного. Этот процесс включает несколько этапов (рис. 1): гликолиз, цикла Кребса и окислительное фосфорилирование (с переносом электронов в митохондриях). При анаэробном дыхании цепи переноса электронов, встроенные в мембрану, тоже есть, только вот финальным акцептором электронов является не кислород, а другие органические и неорганические молекулы. Оно распространено у бактерий и иногда может активироваться у растений (см. статью «Особая диета: молекулярный водород три раза в день, ионы сульфата перед едой» [8]).
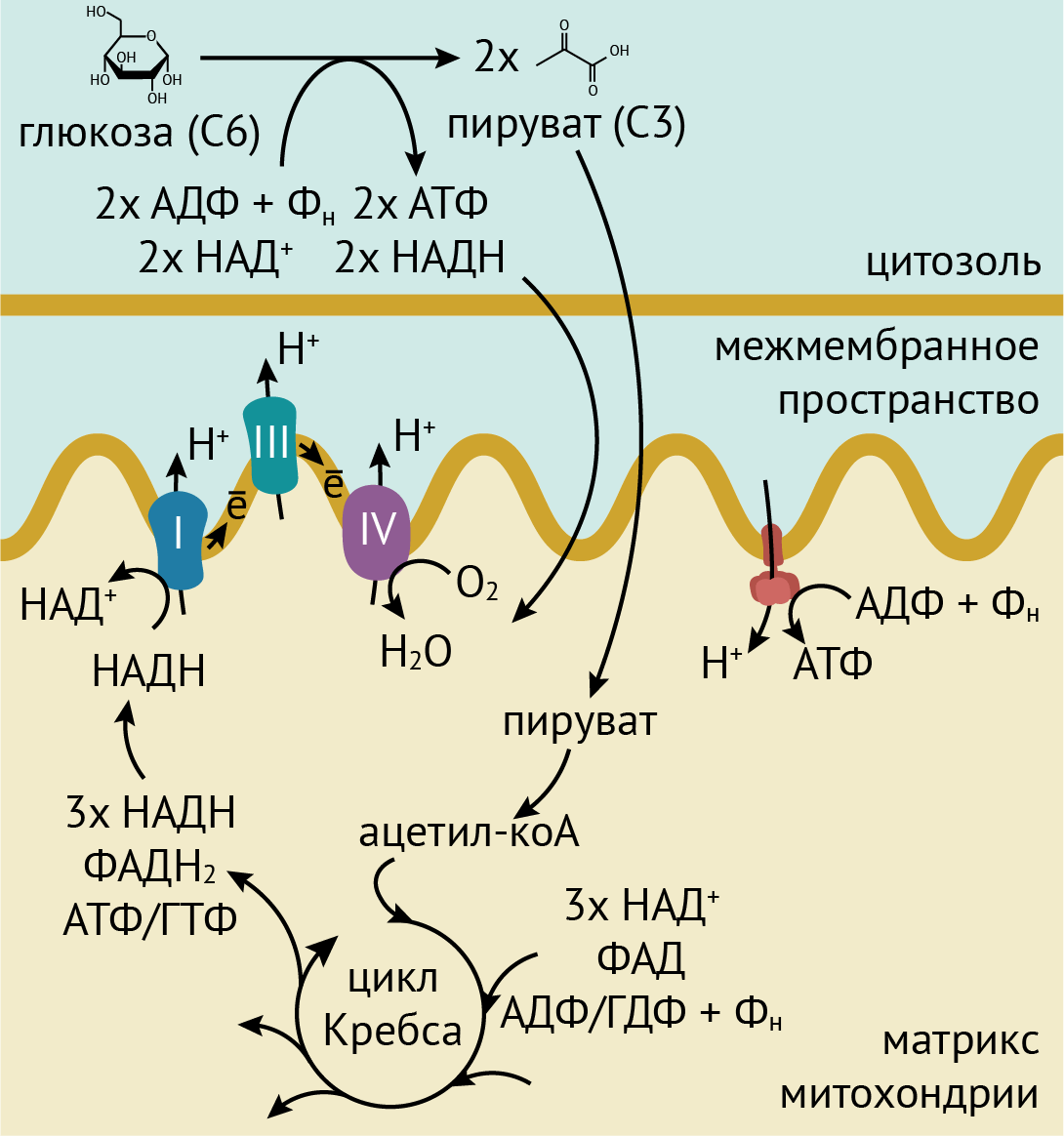
Рисунок 1. Схема дыхания. Сначала глюкоза через ряд превращений в гликолизе превращается в две молекулы пирувата. При этом, в частности, получаются две молекулы АТФ и две молекулы НАДH. Обе молекулы очень важны для энергетических процессов в клетке. Фактически, мы дышим ради получения энергетических молекул. Гликолиз происходит в цитоплазме, после чего пируват импортируется в митохондрии. Там он окисляется до ацетил-кофермента А и вовлекается в цикл Кребса, в ходе которого окисляется до углекислого газа. При этом образуются, в частности, три молекулы НАДН (из НАД+), одна молекула ФАДН (из ФАД — флавинадениндинуклеотида) и одна молекула АТФ или ГТФ. Именно молекулы НАДН и ФАДН важны для следующей стадии дыхания — цепи переноса электронов. Дело в том, что в мембрану митохондрий встроен ряд белков и коферментов, которые могут передавать электроны соседям по цепочке (за счет разности потенциалов). При этом некоторые белки отнимают протоны у НАДН и ФАДН и перекачивают их через одну из двух митохондриальных мембран в межмембранное пространство митохондрий. Последний в цепочке таких белков передает электроны на кислород и превращает его в воду. А протоны накапливаются в межмембранном пространстве митохондрий и закачиваются обратно внутрь митохондрий белком АТФ-синтазой, который, как видно из названия, при этом синтезирует главную энергетическую молекулу клетки — АТФ. Она используется для многих процессов в клетке.
иллюстрация Михаила Гурьева
Гликолиз и цикл Кребса особенно важны для нас, поскольку именно они выходят из строя во многих заболеваниях и вызывают эпигенетические изменения. Они, по сути, не меняются, но меняется баланс метаболитов — одних становится меньше, а других больше, — вот это-то и ведет к эпигенетическим нарушениям. А еще важный продукт цикла Кребса — ацетил-коА — является главным донором ацетильных групп, в том числе и для ацетилирования гистонов, которое, как мы помним, служит меткой активации хроматина.
Отличия метаболизма растений
У растений, помимо аэробного дыхания, есть еще одна цепь переноса электронов, встроенная в мембраны тилакоидов (компартментов внутри хлоропластов) и связанная уже с фотосинтезом. В ней есть два комплекса, способные поглощать свет, причем один из них также разлагает воду до кислорода и протонов (H+). Протоны при этом оказываются внутри тилакоидов, и создаваемое ими напряжение используется АТФ-синтазой, как ротором, для производства АТФ.
А еще растения могут фиксировать углекислый газ, создавая из него органическое вещество. Есть специальный фермент — рибулозобисфосфаткарбоксилаза, который фиксирует CO2 и пришивает его к рибулозобисфосфату [9]. Потом в процессе цикла Кальвина шестиуглеродный продукт расщепляется до двух трехуглеродных, которые затем в цикле превращаются в пятиуглеродную молекулу. В процессе затрачивается много молекул АТФ и НАДН (читается как «НАД-аш»). Таким образом растения фиксируют CO2 и питаются, а еще выделяют кислород, что имеет важнейшее значение для нашей биосферы — откуда его еще брать?
Синтез аминокислот, жиров, углеводов и нуклеотидов
Аминокислоты иногда синтезируются из продуктов гликолиза и цикла Кребса. Например, аланин и некоторые другие получаются из пирувата, а глутамат — из ɑ-кетоглутарата. Некоторые аминокислоты синтезируются из других кислот: например, глутамин — из глутамата; лизин, аспарагин, метионин и некоторые другие — из аспартата; а серин, глицин и цистеин — из 3-фосфоглицерата. В особенности, нам нужно обратить внимание на глутамат и метионин — первого бывает больше или меньше нормы в опухолях, а из второго образуется главный донор метильных групп в клетке.
Жирные кислоты синтезируются в цитоплазме из ацетил-коА, который экспортируется из митохондрий; в обратном процессе ацетил-КоА, наоборот, образуется — и может служить источником ацетильных групп для модификации гистонов. Метаболизм моносахаридов во многом основан на гликолизе и обратном ему процессе — глюконеогенезе.
Метаболиты в эпигенетике
Метаболиты по-разному влияют на эпигенетику. В основном эффект достигается за счет регуляции гистоновых модификаций: ведь чтобы пришить к гистонам химические группы, их необходимо откуда-то взять. Соответственно, ферменты, регулирующие эти метаболиты, регулируют и гистоновые метки. Вот несколько примеров [10]:
- S-аденозилметионин (SAM) синтезируется из АТФ и метионина и служит донором метильной группы для метилтранфераз, которые модифицируют ДНК и разные белки;
- S-аденозилгомоцистеин (SAH), который остается после переноса метильной группы с SAM, ингибирует метилтрансферазы, обеспечивая обратную связь этому процессу;
- фолат и витамины B6 и B12 усиливают производство SAM;
- ɑ-кетоглутарат — промежуточный продукт цикла Кребса — вместе с ионами железа нужен для деметилирования — снятия метильных групп; иногда для деметилирования используется ФАД [11];
- сукцинат и фумарат — другие промежуточные продукты цикла Кребса, — напротив, ингибируют деметилирование;
- ацетил-КоА является донором ацетильной группы для ацетилаз — белков, навешивающих ацетильные группы на гистоны и другие белки, что также меняет активность хроматина, нейтрализует его положительный заряд и увеличивает его рыхлость;
- бетагидроксибутират может синтезироваться в процессе метаболизма жирных кислот, аминокислот, а также других молекул; он ингибирует гистондеацетилазы класса I;
- отношение количества НАД+ к НАДН регулирует гистондеацетилазы класса III, которые также называются сиртуинами;
- НАД+ используется поли-АДФ-рибозополимеразами, которые навешивают цепи поли-АДФ-рибозы на белки, в том числе гистоны; это, в частности, играет роль в починке ДНК [11];
- АТФ является кофактором для многих молекул на хроматине, в частности, ремоделеров, когезинов и конденсинов.
продолжение следует…
